Udenafil의 적응증 확대
- Top-tier Clinic과 함께 ADPKD의 전임상 시작 -
주주총회에서 안내를 드릴 예정입니다만, 주주총회에 참석하지 못하시는 분들을 위해 사전에 공지해 드립니다.
당사는 현재 미국FDA로부터 “폰탄 환자들의 운동능력 증가”를 위한 신약승인을 받기 위한 임상시험(FUEL-2)을 진행 중에 있습니다. 이와는 별도로 당사는 추가로 다른 질환인 “상염색체 우성 다낭성 신장 질환(ADPKD)”의 치료제로 적응증 확대를 적극 추진 중입니다.
상염색체 우성 다낭성 신장 질환(Autosomal Dominant Polycystic Kidney Disease, ADPKD)은 신장에 수많은 낭종이 생기는 유전 질환으로, 발생된 낭종은 점차 커지면서 신장 조직을 손상, 시간이 지남에 따라 신장 기능을 저하시킵니다. ADPKD가 진행됨에 따라 결국 많은 환자들은 말기에는 생존을 위해 투석이나 신장 이식이 필요하게 되는 희귀 신장 질환입니다.
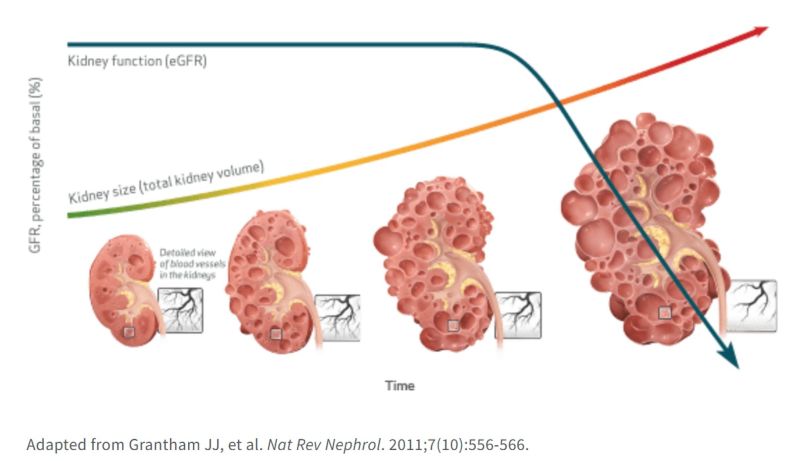
ADPKD 진행은 비정상적인 cAMP 신호 전달 및 손상된 산화질소(NO) 경로와 관련이 있는 것으로 알려져 있습니다.
당사의 Udenafil은 cGMP 신호를 개선하여 잠재적으로cAMP/cGMP 균형을 복원하여 낭종 성장과 섬유증을 억제할 것으로 예상하고 있습니다. 또한 한 연구에 따르면 PDE5 inhibitor가 낭종 성장, 염증 및 섬유증을 감소시켜 핵심 ADPKD 병리를 해결할 수 있는 잠재력을 가지고 있음을 보여주고 있습니다.
ADPKD는 다른 신장 질환에 비해 상대적으로 적은 인구가 영향을 받기 때문에 희귀 질환으로 분류되어 있으며 ADPKD의 미국내 환자수는 대략 14만명으로 추정됩니다. 상염색체 우성으로 유전되기 때문에 자손에게 질병이 전달될 확률이 50%에 달하며, 이는 여러 세대에 걸쳐 유병률을 높이는 원인이 됩니다.
현재 FDA에서 승인한 ADPKD 치료제는 오츠카제약의 Jynarque ®(톨밥탄)이 유일합니다. 톨밥탄은 신장 기능 저하와 낭종 성장을 늦출 수 있지만 간 손상 위험 증가와 정기적인 간 모니터링 필요 등의 부작용이 있습니다. 이러한 부작용과 높은 비용으로 인해 톨밥탄은 일반적으로 질병이 빠르게 진행되는 환자에게만 제한적으로 사용되고 있습니다. * 2024년 Jynarque®(톨밥탄) 매출 : $1.8B(약2.6조원)
ADPKD 환자를 위한 치료제로서 Udenafil 개발은, 상당한 미충족(unmet) 수요가 있는 만큼 시장 잠재력이 충분하다고 판단하고 있습니다.
이에 당사는 세계 최고 권위의 임상병원의 전임상 개발 센터와 전임상을 시작하였으며, 우리의 새로운 Pipeline으로 적극 추진, 진행해 나갈 방침입니다.
현재는 전임상 시작 단계이지만, 그 동안 다른 적응증 개발을 위해 진행되었던 많은 임상 시험들에서 축적된 자료와 본 질환이 희귀질환임을 감안할 때 단축된 임상단계로 임상개발이 신속히 진행될 것으로 판단되고 있습니다.
향후 개발일정을 포함한 추진경과 등에 대해서는 주주님들과 공유해 나가겠습니다.
내일 주주총회 자리에서 뵙겠습니다.